محصولات
فرمولاسیون
ادتا (2سدیم، 4 سدیم) EDTA.2Na
ادتا ( EDTA ) چیست؟
نمکهای سدیم EDTA، ترکیبات شناختهشدهای با کاربرد در صنایع شوینده، کشاورزی، غذایی و همینطور پتروشیمی بهشمار میروند.
ا.د.ت.ا یا « اتیلن دی آمین تترا استیک اسید »، عاملی کیلیتساز و کمپلکسدهنده است که با بسیاری از کاتیون های فلزی، پیوند برقرار کرده و آنها را به دام میاندازد. در این صفحه، پس از تحلیل ساختار ادتا از منظر شیمیایی، خواص فیزیکی-شیمیایی ترکیب و همینطور کاربردهای مختلف آن بهتفصیل بررسی میشود. در نهایت، توضیحات مختصری از ملاحظات زیستمحیطی مربوط به ترکیب ارائه خواهد شد.
جدول مشخصات ادتا:👇
ادتا ( EDTA ) |
ادتا 2 سدیم |
ادتا 4 سدیم |
| 🔴 شکل ظاهری : | پودر سفید رنگ | پودر سفید رنگ |
| 🔵 pH : | 5 – 4 | 11.5 – 10.5 |
| 🔴ماده فعال : | MIN 99 | MIN 99 |
میتوانید مشخصات کامل ادتا رو در ادامه بخوانید:👇
مشخصات کالا
| شکل ظاهری | پودر سفید رنگ |
|---|---|
| درصد خلوص | Min 99.0 |
| درصد کلراید(Cl) | Max 0.01 |
| درصد سولفات(SO4) | Max 0.05 |
| آهن (ppm) | Max 10 |
| pH | 4.0-5.0 |
معرفی و اطلاعات کلی
معرفی ادتا ( edta ) :
« دیسدیم اتیلن دیآمین تترا استیک اسید »، نوعی پلیکربوکسیلیک اسید آمیندار است که در آن دو پروتون (H+ )از مجموع چهار پروتون اسیدی ساختار، بهوسیلۀ سدیم خنثی شده است. شهرت اصلی نمکهای سدیم EDTA مرهون توانایی قابل توجّه این ترکیب در تشکیل کیلیتهای فلزی است. به بیان دقیقتر، جفتالکترونهای ناپیوندی اتمهای نیتروژن و اکسیژن ساختار برهمکنشی کئوردیناسیونی با یونهای فلزی محیط نشان میدهند که به تشکیل پیچیدههای فلزی میانجامد. این خاصیت ویژۀ ادتا، سبب استفادۀ گسترده از این ترکیب بهعنوان عامل نگهدارنده، کاهندۀ سختی آب و همینطور عامل کیلیتدهنده در صنایع مختلف شده است. افزونبراین، کیلیتهای فلزی EDTA در صنایع غذایی و کشاورزی بهعنوان عامل غنیسازی محصول مورد نظر بهکار گرفته میشود.
مشخّصات ظاهری ادتا
از منظر ظاهری، نمکهای سدیم EDTA، عموماً بهصورت پودری بلورین و سفیدرنگ عرضه میشوند. نمکهای سدیم EDTA در آب محلولاند. میزان حلالیّت ترکیب در آب، بهطور مستقیم وابسته به تعداد اتمهای سدیم حاضر در محصول است.
ساختار شیمیایی و سازوکار عملکرد ادتا 2 سدیم و ادتا 4 سدیم:
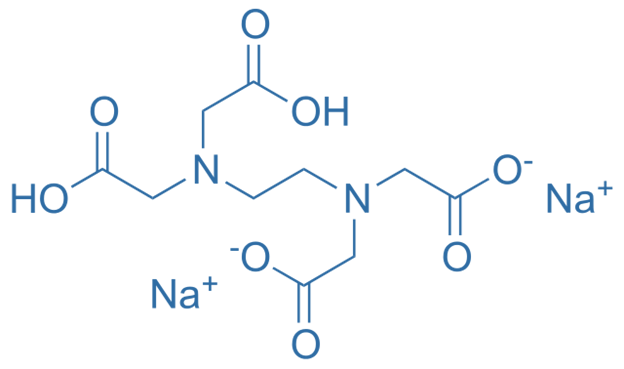
بهطور عمومی، EDTA با فرمول شیمیایی C10H16N2O8 نمایش داده میشود. هنگامی که دو اتم هیدروژن اسیدی از ساختار اتیلن دیآمین تترا استیک اسید، بهوسیلۀ سدیم جایگزین شوند، به نمک حاصل EDTA-Na اطلاق میشود. از منظر صنعتی، EDTA عموماً به صورت خنثیشده با 2 اتم سدیم (EDTA-2Na) و یا 4 اتم سدیم (EDTA-4Na) عرضه میشود.
EDTA شامل یک زنجیرۀ هیدروکربنی اشباع، چهار گروه کربوکسیلات و دو گروه آمین است. یکی از ویژگیهای منحصربهفرد این ترکیب، انعطافپذیری قابل توجّه هندسۀ ساختار است. به بیان دقیقتر، زنجیرۀ اتیلنی (-CH2-CH2-) که از پیوندهای یگانۀ سیگما شکل یافته است، تشکیل ایزومرهای فضایی گوناگون را میسّر میسازد.
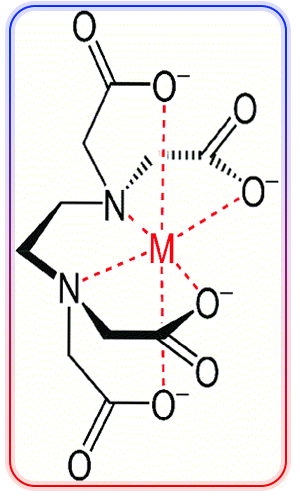
انعطافپذیری هندسی EDTA موجب میشود که ساختار بتواند در شکلی مشابه با پنجۀ پرندگان به دور یونهای فلزی آرایش یابد و واکنش دهد. چرخش ساختار حول زنجیرۀ اتیلنی سبب تسهیل فرآیند بهدام انداختن یونهای فلزی و تشکیل پیچیدههای فلزی (کمپلکس) میشود. ادتا در حقیقت ترکیبی 6 دندانه است که میتواند از طریق گروههای کربوکسیلات و همینطور آمینهای واقع بر زنجیر، با فلزهای سنگین واکنش دهد و متعاقباً پیچیدههای فلزی تشکیل دهند. لازم به توضیح است که انعطافپذیری بالای ساختار، اصلیترین عاملی است که EDTA-Na میتواند بر چالشِ ممانعت فضایی ساختارهای بزرگ غلبه کند و با آنها واکنش دهد.
ساختار نهاییِ پیچیدۀ فلزی تشکیلشده عموماً 8وجهی (اکتاهدرال) است؛ در این ساختار مولکول فلزی در مرکز قرار دارد و بهوسیلۀ لیگاندها احاطه شده است. این ساختار هندسی عموماً پایداری بالایی دارد که استفاده از این ترکیب را در کاربردهای وابسته به کاهش سختی، بیشازپیش ساخته است.
اضافه شدن گروههای سدیم به ساختار EDTA انحلالپذیری ترکیب را در محیط آبی افزایش میدهد و pH را تا حدودی به سمت منطقۀ خنثی، تغییر میدهد. این افزایش انحلالپذیری، حرکت مولکول در محیط آبی را تسهیل میکند و بهنوعی به انعطافپذیری ساختار در محیط آبی یاری میرساند.
ساختار شیمایی ادتا (EDTA)
پیکربندی مشابه پنجه برای ادتا (EDTA)
تفاوتهای EDTA-2Na و EDTA-4Na
از منظر کاربردی، هر دو نوع نمک سدیم EDTA توانایی کاربردی یکسانی در تشکیل کیلیت با فلزّات گوناگون دارند. مهمترین تفاوت این دو نوع نمک، محدودۀ pH کاربری و همینطور میزان حلّالیّت آنها در آب است. چنانچه در بخش پیشین به آن پرداخته شد، EDTA حلّالیّت اندکی در آب دارد. افزودن گروههای سدیم به این ترکیب، به افزایش قابل توجّه حلّالیّت EDTA در آب میانجامد.
EDTA بهواسطۀ ماهیت اسیدی خویش، نوعی ترکیب حسّاس به pH بهشمار میرود. افزودن گروههای سدیم به ساختار، این حسّاسیّت به pH را کاهش میدهد بهطوریکه EDTA-2Na نسبت به ترکیب خالص EDTA حسّاسیّت کمتری به pH دارد و EDTA-4Na نسبت به هر دو ترکیب، عملکرد بهتری در pHهای خنثی دارد.
نمک EDTA-2Na، دارای pH در محدودۀ 4-5 است درحالیکه مقدار pH نمک EDTA-4Na بین 10 تا 12 متغیّر است. مطابق با این موضوع، EDTA-2Naعملکرد بهتری در محلولهای اسیدی از خویش نشان میدهد در شرایطی که، محلولهای خنثی و قلیایی، سازگاری بیشتری با EDTA-4Na دارند.
کاربردها و صنایع وابسته ادتا (EDTA)
1- نسّاجی
شستوشوی محصولات نسّاجی با آب سنگین، از یکسو به رسوب این ترکیبات بر سطح پارچه میانجامد و از سوی دیگر، حضور یونهای فلزی در آب میتواند به واکنش با مولکولهای مادّۀ رنگزا و متعاقباً تغییر رنگ پارچه منجر شود. ازاینروی، استفاده از EDTA، سبب از میان بردن یونهای فلزی فعال، کاهش سختی آب و متعاقباً بهبود فرآیندهای شستوشو میشود.
بر اساس همین منطق، استفاده از این ترکیب در خود فرآیند رنگرزی نیز به یکنواختی بیشتر رنگ میانجامد. ازاینروی، بهکارگیری EDTA، چه در هنگام رنگرزی و چه در هنگام شستوشو، به یکنواختی و همینطور نرمی بیشتر سطح پارچه میانجامد.
2- صنایع غذایی
افزودنیهای مبتنی بر “ادتا ” بهطور گسترده در صنایع غذایی به کار گرفته میشوند. پژوهشهای گوناگون حاکی از آناند که کیلیتهای آهنی حاوی EDTA(ادتا) جذب بالاتری در بدن دارند. براینمبنا، در برخی از کشورها، استفاده از FeNaEDTA در غنیسازی فرآوردههای غذایی مجاز است.
استفاده از ترکیبات مبتنی بر EDTA، افزون بر کاربرد در غنیسازی مواد غذایی با آهن، کلسیم و غیره، به حفظ طعم و بوی محصولات غذایی نیز کمک میکند و از رخ دادن واکنشهای اکسیداسیون ناخواسته میکاهد. بهعنوان نمونه، «کلسیم دیسدیم ادتا»، کاربرد وسیعی در صنایع غذایی بهعنوان افزودنی طعمدهنده و آنتیاکسیدان دارد.
3- ادتا در صنایع بهداشتی، آرایشی، شوینده
از اصلیترین مصارف ” ادتا “، استفاده در شویندهها، شامپوها و محصولات آرایشی، بهداشتی است. در فرمولاسیون بسیاری از محصولات یادشده، از سورفکتانتهای مختلف استفاده میشود. این سورفکتانتها، بهویژه سورفکتانتهای آنیونی، مستعد واکنش با کاتیونهای فلزی موجود در آب اند. چنین واکنشهایی افت محسوس عملکرد سورفکتانتها را در پی دارد.
استفاده از ادتا(دیسدیم اتیلن دیآمین تترا استیک اسید) در فرمولاسیون چنین ترکیباتی سبب میشود که:
- طول عمر محصول افزایش یابد و شرایط نگهداری آن تسهیل شود.
- عملکرد سورفکتانتها تحت تأثیر سختی آب قرار نگیرد.
- هنگام شستوشوی پارچه یا لباس، یونهای فلزات سنگین رنگ پارچه را تغییر ندهند.
با توجّه به توضیحات بالا، ” ا.د.تت.ا ” در فرمولاسیون بسیاری از محصولات حوزۀ شوینده، بهداشتی و آرایشی بهکار گرفته میشود.
4- شیرینسازی گاز
نمک آهن ادتا ، یکی از ترکیباتی است که به حذف گاز H2S از جریان گاز طبیعی و متعاقباً شیرینسازی گاز کمک میکند. در این فرآیند، طی واکنش هیدروژن دیسولفید با کمپلکس آهن و EDTA، آهن سهظرفیتی به آهن دوظرفیتی تبدیل میشود و هیدروژن دیسولفید نیز به گوگرد و گاز هیدروژن تجزیه میشود.
5- پزشکی- دارویی
یکی از کاربردهای سدیمادتات یا کلسیمسدیمادتات، جذب قلع یا جیوه از بدن است. استفاده از این ترکیب برای مقابله با مسمومیّتهای قلع و جیوه، روشی تأییدشده و پر استفاده برای نجات بیمارانی است که دچار مسمویّتهای خطرناکِ بلع یا جذب فلزات سنگین شدهاند.
از سوی دیگر، EDTA بهطور گسترده در تحلیل آزمایش خون و بهعنوان ترکیب ضدّ انعقاد بهکار گرفته میشود. کاتیون Ca2+ بهعنوان کاتالیزور، نقش مهمّی در فرآیند انعقاد خون دارد. بر این اساس، EDTA با تشکیل کیلیت فلزی و خنثیسازی کاتیون کلسیم، انعقاد نمونههای آزمایش خون را به تعویق میاندازد. این امر، امکان انجام تحلیلها و آزمایشهای متفاوت روی نمونه را میسّر میسازد.
6- کشاورزی
بهکارگیری کیلیتهای فلزی حاوی سدیم، منیزیم، مس، روی و آهن به درون خاک سبب باروری و غنیسازی خاک میشود. در سالیان اخیر استفاده از کودهای حاوی نمکهای مختلف EDTA رشد قابل توجّهی داشته است. یکی از ویژگیهای منحصر به فرد استفاده از چنین نمکهایی، رهایش مداوم عناصر فلزی است. این ویژگی به جذب بهینۀ یونهای فلزی کمک شایانی میکند.
7- ادتا در صنایع نفت، گاز، پیتروشیمی
یکی از مشکلات متداول در فرآیند حفّاری، رسوب گل حفّاری، بهویژه در لایههای نزدیکتر به حفره است. چنین رسوباتی سبب کاهش دبی خروجی از چاه و متعاقباً کاهش بازدهی برداشت میشود. برای حل این مشکل و فرآیند انگیزش چاه، روشهای متفاوتی پیشنهاد شده است. یکی از کاربردیترین روشهای غلبه بر این مشکل استفاده از ترکیبات کیلیتکننده است. بهکارگیری ترکیباتی مانند EDTA همراه با فرآیند اسیدی، سبب پدید آمدن تَرَکها و اصطلاحاً کرمچالههایی در بستر سنگ میشود. این موضوع، بهویژه در مورد سنگهای کربناتی به افزایش قابل توجّه بازدهی برداشت میانجامد.
علاوه بر فرآیند انگیزش خاک، استفاده از ترکیبات کیلیتساز منجر به جذب رسوبات فلزی نیز میشود. مطابق با توضیحات پیشین، EDTA با تشکیل کیلیت، به جذب یونها و متعاقباً رسوبات فلزی کمک میکند.
ملاحظات زیستمحیطی ادتا
چنانچه پیشتر نیز اشاره شد، از منظر سلامتی، EDTA و نمکهای سدیم این ترکیب، محصولاتی امن و غیر سمّی بهشمار میروند. سازمان غذا و داروی آمریکا، استفاده از این محصول را در صنایع آرایشی و بهداشتی تأیید کرده است. افزونبراین، در بسیاری از کشورهای اروپایی، استفاده از کیلیتهای فلزی EDTA بهعنوان مکمّل غذایی پذیرفته شده است.
با این وجود دیسدیم اتیلن دیآمین تترا استیک اسید، بهویژه پس از تشکیل پیچیدۀ فلزی، ترکیبی زیستتخریبپذیر بهشمار نمیرود. برهمینمبنا، نمیتوان آن را در زمرۀ ترکیبات دوستدار محیطزیست قرار داد.
ویژگی ها و مزایا دیسدیم اتیلن دیآمین تترا استیک اسید :
- ماده ای بی رنگ
- محلول در آب
- عامل کی لیت کننده
- اصلاح کننده pH
فرم درخواست اطلاعات تخصصی
نیاز به اطلاعات بیشتر در مورد این محصول دارید؟
درخواست اطلاعات بیشتر
گواهینامه ها

NACI

ISO 45001

ISO 14001

ISO 9001

isiri